Potentieel kunnen er in de zorg veel kosten worden bespaard door dure geneesmiddelen na het verlopen van hun patent in te ruilen voor een goedkoper alternatief. Maar dalen de kosten inderdaad bij een lagere medicijnprijs? Een analyse gemaakt in een Nederlands ziekenhuis.
In het kort
– Vervanging van dure medicijnen waarvan het patent verlopen is veroorzaakt een daling in de medicatiekosten per patiënt.
– De totale medicijnkosten dalen echter niet, omdat er met de goedkopere medicijnen meer patiënten behandeld worden.
Kostenbeheersing in de gezondheidszorg is een groot probleem (Adang en Jeurissen, 2020). De afgelopen jaren zijn de uitgaven aan geneesmiddelen in de medisch-specialistische zorg voortdurend gestegen. Het aandeel dure geneesmiddelen is, in vergelijking met de totale uitgaven aan medisch-specialistische zorg, gestegen van 6,8 procent in 2012 naar 9,5 in 2018. Dit komt vooral door de introductie van nieuwe medicijnen en door een toename van het aantal patiënten (NZA, 2019).
Algemeen wordt er aangenomen dat wanneer een patent op geneesmiddelen verloopt, dit leidt tot een daling van de kosten voor de gezondheidszorg. Verwacht wordt dat een prijsdaling voor dure medicatie, vanwege de beschikbaarheid van niet-gepatenteerde biologische geneesmiddelen (zogenaamde biosimilars) die even effectief zijn, zal gaan leiden tot lagere totale kosten en daardoor een algemene budgettaire verlichting zal creëren. Biosimilars komen na het aflopen van patenten op de markt nadat deze beoordeeld zijn door het Europese Geneesmiddelenagentschap (EMA) en het Nederlandse College ter Beoordeling van Geneesmiddelen (CBG). Onder andere de Initiatiefgroep Biosimilars Nederland stelt (op haar website) dat met deze biosimilars honderden miljoenen euro’s kunnen worden bespaard, die elders in de zorg ingezet kunnen worden.
In dit artikel, gebaseerd op Müskens et al. (2020), onderzoeken we of in Nederland deze verwachte kostenbesparing ook daadwerkelijk optreedt. Hierbij focussen we specifiek op de biologische medicatie voor patiënten met reumatoïde artritis (RA). RA is een van de gebieden waar de introductie van biosimilars bij de behandeling naar verwachting besparingen zal gaan opleveren. Zo maakte de algemeen directeur van de Britse National Health Service (NHS) onlangs bekend dat hij verwacht dat het gebruik van een biosimilar van adalimumab in het Verenigd Koninkrijk 300 miljoen pond (340 miljoen euro) vrijmaakt, dat volgens hem kan worden geïnvesteerd in de algemene patiëntenzorg (Heal, 2018).
Data en methode
Met behulp van een zogenaamde onderbroken-tijdreeksanalyse hebben we binnen een representatief algemeen ziekenhuis in Nederland het effect van de introductie van een biosimilar van het medicijn etanercept op de betaalbaarheid en toegankelijkheid van zorg onderzocht. We kijken daarbij naar RA-patiënten vanaf 2014 tot aan de introductie van de biosimilar, medio 2016, en de periode daarna tot juni 2018. Zie voor verdere details Müskens et al. (2020).
Kosten per gebruiker
Na de invoering van de biosimilar dalen de gemiddelde medicatiekosten per gebruiker significant met 370 euro, gevolgd door een verdere duidelijke afname per kwartaal (ten opzichte van de trend vóór de invoering). Hierdoor is er een significante daling van de gemiddelde medicatiekostencurve per gebruiker (figuur 1).
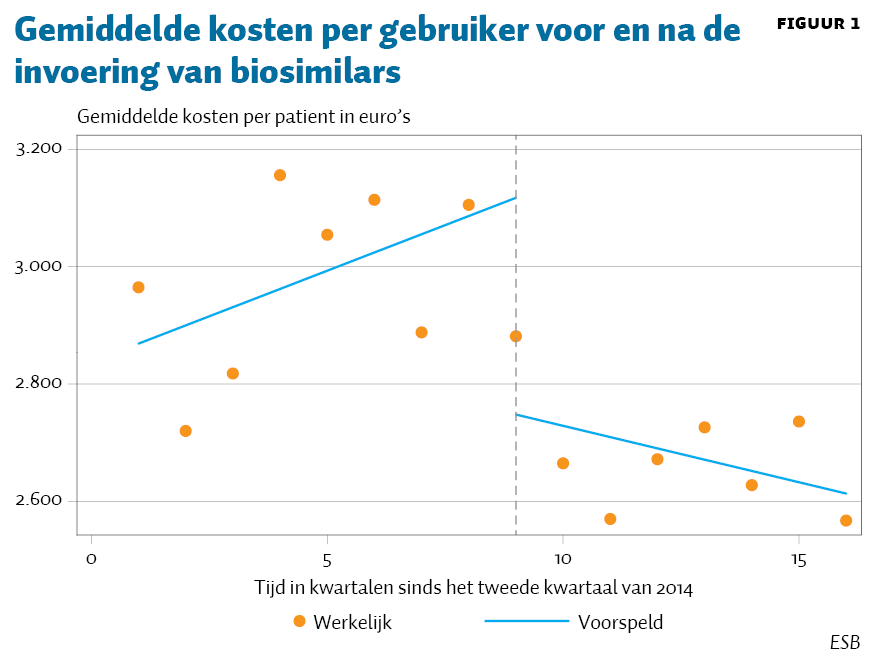
Totale kosten
In het eerste kwartaal na de invoering van de biosimilar was er een statistisch significante daling van 63.020 euro wat betreft de totale gebruikerskosten van dit biologische geneesmiddel binnen het betreffende ziekenhuis. De stijgende trend na de introductie van de biosimilar week echter niet af van de trend voorafgaande aan de introductie – en na drie kwartalen waren de totale medicatiekosten weer op het oorspronkelijke introductieniveau (figuur 2). Als gevolg van deze uitgebleven trendbreuk waren er geen vrijelijk beschikbare kostenbesparingen, en was er dus ook geen algemene budgettaire verlichting.

Meer patiënten
Dat de totale kosten, ondanks de daling van de gemiddelde kosten, hetzelfde bleven, wordt verklaard doordat er bijna 25 procent meer patiënten met biologische geneesmiddelen werden behandeld. Het betrof hier vooral oudere RA-patiënten, waardoor de gemiddelde leeftijd bij aanvang van het eerste biologische geneesmiddel toenam. In de regel is men juist terughoudend bij het behandelen van oudere patiënten met biologische geneesmiddelen (Tutuncu et al., 2006).
Na de invoering van de biosimilars hadden patiënten ook minder disease-modifying antirheumatic drugs gebruikt alvorens er gestart werd met de dure ‘biological’. Dit duidt erop dat men meer patiënten met biologische middelen is gaan behandelen, maar ook op een enigszins andere populatie.
Conclusie en discussie
Door de introductie van biosimilars dalen de gemiddelde kosten per gebruiker, maar blijven de totale kosten hetzelfde en vertonen dezelfde trend als vóór de introductie omdat er meer patiënten behandeld worden. Er zijn aanwijzingen dat de extra behandelde patiënten een iets andere, veelal oudere populatie betreft.
We kunnen niet uitsluiten dat deze populatie voorheen onderbehandeld werd, maar het is onduidelijk of dit extra behandelen wel doelmatig is. Er was geen vooropgezet plan vanuit de afdeling reumatologie van het desbetreffende ziekenhuis om meer te gaan behandelen.
Dat er kennelijk ‘automatisch’ meer behandeld werd na het introduceren van de biosimilar is verrassend, aangezien de Monitor geneesmiddelen in de medisch-specialistische zorg stelt dat de meeste zorgverzekeraars aangeven met de zorgaanbieders afspraken te hebben gemaakt over een doelmatige inzet van biosimilars (NZA, 2019). Idealiter zou er continu op patiëntniveau gemonitord moeten worden op de effecten van behandelingen als er in het voorschrijfgedrag veranderingen plaatsvinden, zoals de introductie van biosimilars. Dat zou een taak van de voorschrijvers moeten zijn, maar dit gebeurt momenteel niet.
Mogelijk zijn de extra behandelingen het gevolg van perverse prikkels. Als ziekenhuizen een positief onderhandelingsresultaat over de prijs van biosimilars met verzekeraars hebben bedongen, kan dat als prikkel tot meer behandelen werken, aangezien het volumerisico bij de verzekeraar ligt (NZA, 2019).
De resultaten laten in ieder geval zien dat er geen duidelijkheid is omtrent de regievoering op geanticipeerde besparingen in de zorg, of omtrent een doelmatige besteding van middelen bij verandering van bijvoorbeeld voorschrijfgedrag. Daarmee is er een lacune in ons zorgstelsel waardoor potentiële welvaartswinsten niet worden gerealiseerd.
De vraag is welke partij of partijen hier de regie zouden moeten nemen. Vanuit een maatschappelijk perspectief ligt het voor de hand om de regie bij de verzekeraars te leggen. Omdat dit in het verleden echter weinig resultaat heeft opgeleverd, is het wellicht beter om het tot een gezamenlijke verantwoordelijkheid van de verzekeraars en zorgaanbieders te maken. In dat geval kan een deel van de besparingen worden ingezet om de algemene groei in de zorg te bekostigen, en een deel ervan om de kwaliteit van zorg in de zorginstellingen op een doelmatige wijze te verbeteren.

Literatuur
Adang, E. en P. Jeurissen (2020) Kritische houding ten aanzien van innovaties in de zorg noodzakelijk. ESB, 105(4785), 198–200.
Heal, A. (2018) NHS replaces highest-spend drug with £300m cheaper alternative. The Guardian, 26 november.
Müskens, W.D., S.A. Rongen-van Dartel, P.L.C.M. van Riel en E.M.M. Adang (2020) Does Etanercept biosimilar prescription in a rheumatology center bend the medication cost curve? The Journal of Rheumatology, te verschijnen.
NZA (2019) Monitor geneesmiddelen in de medisch specialistische zorg januari 2019. Nederlandse Zorgautoriteit.
Tutuncu Z., G. Reed, J. Kremer en A. Kavanaugh (2006) Do patients with older-onset rheumatoid arthritis receive less aggressive treatment? Annals of the Rheumatic Diseases, 65(9), 1226–1229.
Auteurs
Categorieën







